普利制药苯磺顺阿曲库铵注射液获得美国上市许可
海南普利制药股份有限公司(以下简称“普利制药”或“公司”)于近日收到美国食品药品监督管理局(以下简称“FDA”)签发的苯磺顺阿曲库铵注射液的上市许可。
这标志着普利制药具备在美国销售苯磺顺阿曲库铵注射液的资格,将对公司拓展美国市场带来积极影响。

药品基本信息
药品名称:苯磺顺阿曲库铵注射液
适应症:(1)用于辅助成人及1个月到12岁儿童患者气管插管的全身麻醉;(2)推注或输注给药维持成人及2到12岁儿童患者手术期间的骨骼肌松弛;(3)适用于成人ICU的机械通气。
剂型:注射剂
规格:20mg/10mL
ANDA号:216538
生产企业:海南普利制药股份有限公司
苯磺顺阿曲库铵是一种非去极化神经肌肉阻断剂,通过抑制神经肌肉的传导而对乙酰胆碱起拮抗作用。
苯磺顺阿曲库铵最早由GSK在1989年合成,之后代理权转让给Abbvie,由Abbvie进行临床开发。1995年12月Abbvie Inc.开发的原研药苯磺顺阿曲库铵注射液Nimbex®(EQ 2 mg base/mL)和Nimbex Preservative Free®(EQ 10 mg base/mL和EQ 2 mg base/mL)首先在美国获批上市。1995年12月Glaxosmithkline开发的Nimbex在英国获批,随后Nimbex也在其他欧盟国家获批。2004年,Glaxosmithkline的苯磺顺阿曲库铵注射液获批进入中国市场,具有巨大的市场潜力。
美国为全球第二大市场
IMS数据显示,2022年全球苯磺顺阿曲库铵注射剂销售额达1.83亿美元。其中,美国为全球第二大市场,销售额3452万美元,占比19%。此次布苯磺顺阿曲库铵注射液的美国FDA获批,具有较好的销售预期。
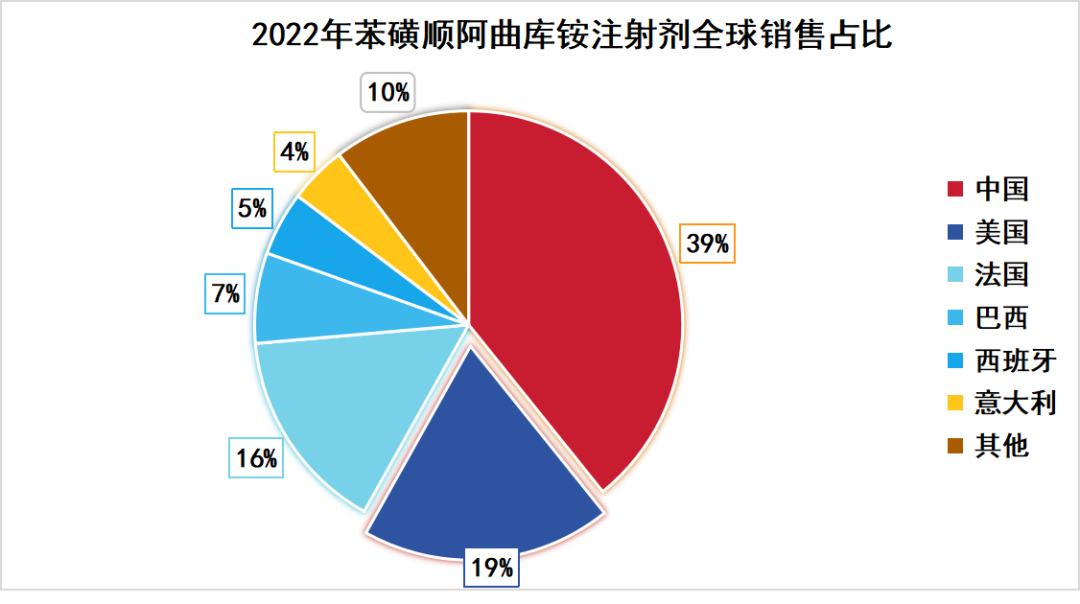
中国为苯磺顺阿曲库铵注射剂的全球第一大市场,2021年苯磺顺阿曲库铵注射液纳入第五批国家集中带量采购。普利制药提前布局苯磺顺阿曲库铵注射液的美国FDA申报,如今迎来收获期,这是普利制药在2024年获得的第5张美国ANDA。
普利制药国际市场销售产品“适销对路”,是普利制药已经上市和正在注册管线上注册品种的显著特点。到目前为止,普利制药获得欧美等国际注册的品种,在订单下达后均能实现出口创汇!

 首页
首页