海南普利制药股份有限公司(以下简称“普利制药”或“公司”)于近日收到美国食品药品监督管理局(以下简称“FDA”)签发的布立西坦注射液的暂时性批准,标志着待2026.02.21由UCB公司持有的布立西坦化合物专利US6911461B2到期失效后,公司即可转为正式批准,届时将具备在美国销售布立西坦注射液的资格,将对公司拓展美国市场带来积极影响。
这已是普利制药2024年获得的美国第4张ANDA批件,此次获批不仅彰显了公司在抗癫痫领域的卓越实力,更标志着普利制药在美国市场抗癫痫管线继左乙拉西坦注射用浓溶液、拉考沙胺注射液之后的产品布局迈出了又一战略性的先导步伐。
药品名称:布立西坦注射液
适应症:1个月及以上患者部分发作性癫痫的治疗
剂型:注射剂
规格:50mg/5mL
ANDA号:218249
生产企业:海南普利制药股份有限公司
第三代抗癫痫药,市场潜力巨大
布立西坦最早由UCB制药研发,2016年1月UCB开发的原研药布立西坦注射液Briviact首先在欧盟批准上市,2016年2月获准在美国上市,尚未在中国获批上市。UCB公司持有的布立西坦化合物专利US6911461B2仍在有效期内,将于2026-02-21到期失效,目前该品种在美国无正式获批的仿制药。此次普利制药收到FDA签发的布立西坦注射液的暂时性批准,不仅彰显了公司在抗癫痫领域的卓越实力,更标志着普利制药在美国市场抗癫痫管线继左乙拉西坦注射用浓溶液、拉考沙胺注射液之后的布局迈出了战略性的先导步伐。
布立西坦(又名布瓦西坦)作为第三代抗癫痫药,适用于治疗癫痫部分发作。布立西坦是左乙拉西坦的类似物,对大脑中的突触小泡蛋白2A(SV2A)表现出选择性和高亲和力。突触小泡蛋白2A是在神经元和内分泌细胞中在突触前水平发现的跨膜糖蛋白。尽管该蛋白的确切作用尚待阐明,但已表明它可调节神经递质的胞吐作用。与SV2A的结合应为布立西坦抗惊厥活性的主要机制。
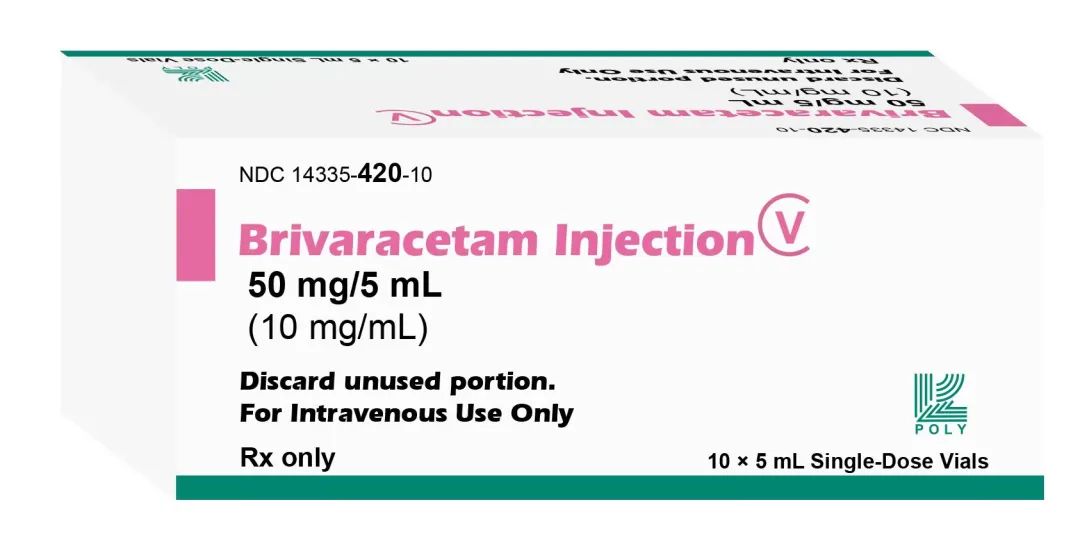
相比左乙拉西坦,对抑制癫痫部分发作的重要位点的选择性和结合亲和力更高,具有更快的脑部渗透速度,抗癫痫潜力和有效性更高。
左乙拉西坦与布立西坦结构对比图
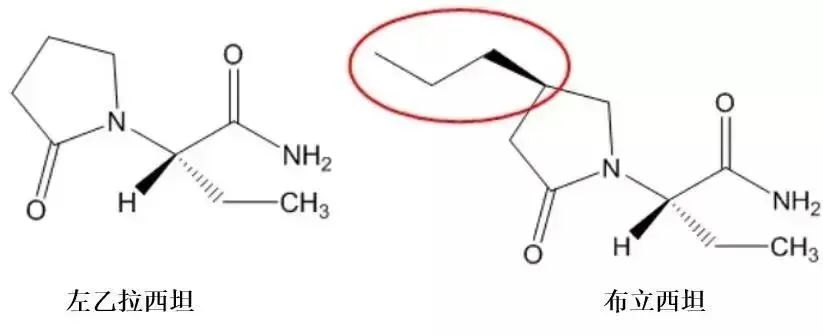
根据IMS数据,布立西坦自2016年获批上市起市场呈现快速增长状态,2023年全球销售额达到6.67亿美元,其中美国市场产出约4.5亿美元,占比67%,为全球第一大市场。
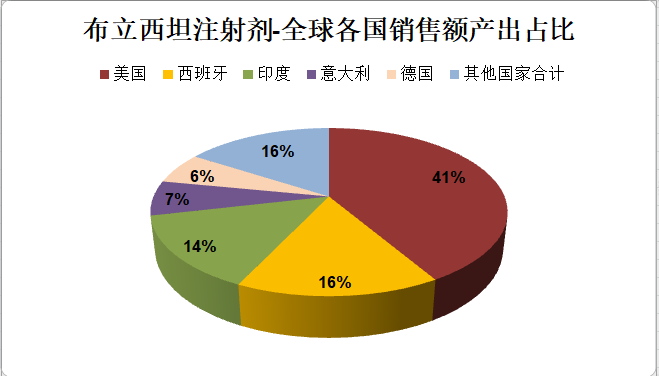
其中,美国市场的布立西坦注射剂同样表现优异,销售额占比全球41%,排名第1。作为第三代同时兼具注射剂型和口服剂型的新型抗癫痫药,布立西坦的市场潜力巨大。

 首页
首页