海南普利制药股份有限公司旗下的全资子公司浙江普利药业有限公司于近日收到国家药品监督管理局(以下简称“NMPA”)所签发的胺碘酮注射液的药品注册批件,视为通过一致性评价批准上市,将为拓展国内市场带来积极影响。

普利制药胺碘酮注射液批件:3ml:150mg、18ml:900mg
普利制药此次胺碘酮注射液在中国获批上市的有两种规格:3ml:150mg、18ml:900mg。公司胺碘酮注射液为中美双报、原料制剂一体化品种,质量安全有保证,将为国内患者提供高品质的用药选择。
胺碘酮基本情况
盐酸胺碘酮属于Ⅲ类抗心律失常药物,是一种多离子通道阻滞剂,因此,同时具有Ⅰ、Ⅱ、Ⅳ类抗心律失常药物的作用。静脉用胺碘酮,更多表现为Ⅲ类药物之外的作用,即钠通道阻滞、β受体阻滞及钙通道阻滞作用。通过抑制这些离子通道带来的电生理效应包括抑制窦房结、房室交界区的自律性,减慢心房、房室结、房室旁路传导及延缓心房肌、心室肌的动作电位时程和有效不应期,由此带来广谱抗心律失常作用,,是临床抗心律失常的一线用药。
盐酸胺碘酮于1961年首次合成,在1974年被发现对心律失常有用。盐酸胺碘酮于1966年12月在法国首次获准用于口服制剂,并于1976年4月在法国获批用于注射。1985年其口服制剂以商品名Cordarone在美国上市,持证商为Wyeth Pharmaceuticals Inc,用于治疗心律失常。1995年Cordarone注射液在美国、加拿大上市。Cordarone注射液目前上市国家包括英国、法国、意大利、荷兰等。中国在2007年04月27日批准了可达龙 (Cordargne)注射液原研进口申请。
胺碘酮注射剂市场规模
普利制药胺碘酮注射液完成技术研发后,逐步向国内外多个市场提交了产品的上市申请,已于2024年9月获得美国FDA上市批准及本次的中国NMPA上市批准。除以上获批国家外,胺碘酮注射液其他市场的注册工作正在持续推进中,目前在审国家有加拿大,待递交国家有泰国、菲律宾。
根据IQVIA的数据显示,2023年全球盐酸胺碘酮针剂的销售额约为8.9亿元人民币,近几年增长率呈稳定增长趋势。其中美国市场占据了54%的份额,为全球最大的市场,中国市场占据了17%的市场份额,为全球第二大市场。中国、美国为胺碘酮主要市场。
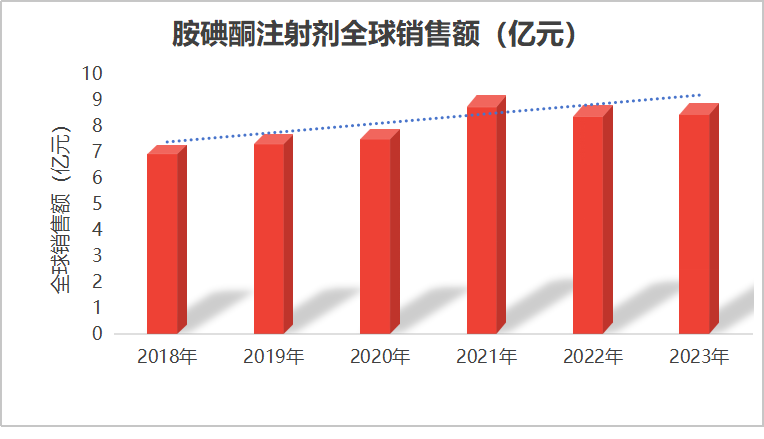
数据源于IQVIA数据库
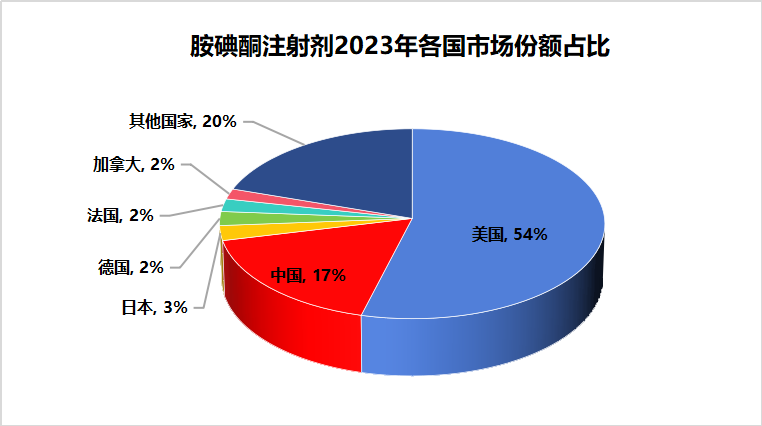
数据源于IQVIA数据库
据米内网数据显示,中国国内2023年胺碘酮注射剂在医院销售额约为1.9亿元,810万支。近三年其销售额呈稳定上升趋势。
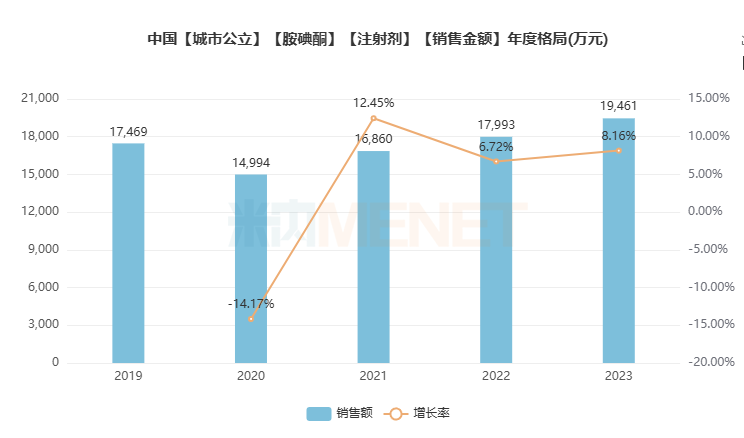
数据源于米内网数据库
在中国城市公立医院、县级公立医院、城市社区中心及乡镇卫生院(简称中国公立医疗机构)终端,抗心律失常药品2023年销售额超过5亿元,2023年有11.28%的增长。胺碘酮同通用名药品销售额达3.17亿元,占据了抗心律失常药将近60%的市场份额,已成为该类别TOP1品种,胺碘酮为抗心律失常最主要的一线治疗用药。
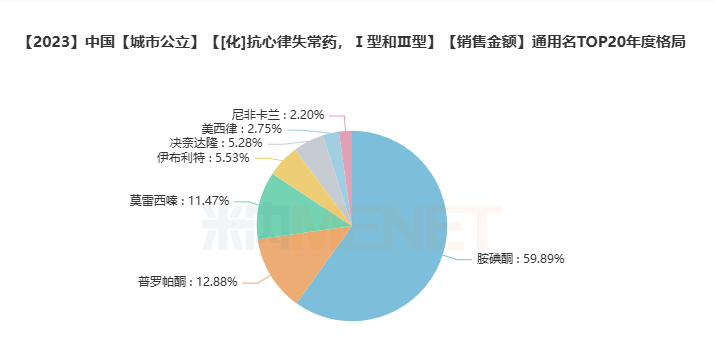
数据源于米内网数据库
中美双报、原料制剂一体化品种
胺碘酮注射液为中美双报品种,国内与美国市场共用一条生产线,同质量标准,同产品品质,将为国内患者提供高品质的用药选择。
盐酸胺碘酮注射液是普利制药开发的原料制剂一体化品种。盐酸胺碘酮原料为中美欧申报,中国(登记号:Y20210001090)和欧洲(CEP证书编号:R0-CEP 2021-481-Rev 00)已经获批;美国盐酸胺碘酮原料与制剂关联评审(DMF号:036163),同时获得批准。
作为原料制剂一体化品种,普利制药的盐酸胺碘酮注射液不会受制于原料药市场,可稳定保障临床供应。

海南普利制药股份有限公司1992年成立于海口,是中国医药制剂国际化先导企业和国家工信部智能制造示范企业,已被国家工信部纳入工业转型升级中国制造2025年儿童药重点项目企业。2017年创业板上市后,短短3年已成为中国上市公司科技创新百强企业。
普利制药拥有海口、杭州和安庆三个国际化高端制造基地和产业化技术中心,是国内为数不多的,符合欧美cGMP标准的生物制药上市公司。
未来,普利制药将一如既往地实施“先进高端制造, 面向国内国际”的全球战略,持续不断研发更多更好的药物;走向世界,为民族医药工业的强大持续作出贡献,让中国老百姓用上出口欧美的高品质健康品。

 首页
首页